MI SELECCIÓN DE NOTICIAS
Noticias personalizadas, de acuerdo a sus temas de interés
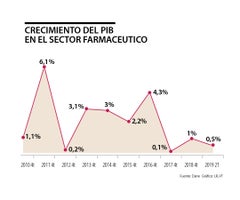
Farmacéuticas presentan de manera anónima las preocupaciones que tienen ante la gestión de trámites que realiza el Invima
Los registros y solicitudes sanitarias de medicamentos, que las industrias farmacéuticas deben tramitar, son permisos que se otorgan para la comercialización y distribución de los mismos. Según la Organización Mundial de la Salud (OMS), estos permisos se hacen necesarios a razón de mantener un control sobre todos los productos, tanto medicinales como cosméticos y alimenticios, que en últimas serán de consumo común. En Colombia, la entidad encargada de entregar estos documentos es el Invima, pero de un tiempo para acá, las farmacéuticas vienen quejándose de las demoras y de su gestión.
El origen del problema se puede ubicar en agosto de 2018, cuando la Fiscalía General de la Nación, luego de una intensa investigación, logró la captura de 14 funcionarios del Invima que venían recibiendo pagos para la agilización de la expedición y falsificación de registros sanitarios, lo que según la entidad fiscalizadora, representaba un atentado contra la vida de los consumidores.
Con eso, la reputación de la entidad quedó lastimada, y se empezó un proceso de renovación que se intensificó en octubre con el nombramiento de Julio Cesar Aldana como director de la entidad. Esto dejó a la institución en un proceso de reacomodamiento hacia una nueva administración.
Ya casi se va a completar el primer año de Aldana al frente de la entidad, pero de acuerdo con las farmacéuticas, no se ha podido cumplir el mandato del presidente Iván Duque de tener un Invima transparente, ágil y eficiente.
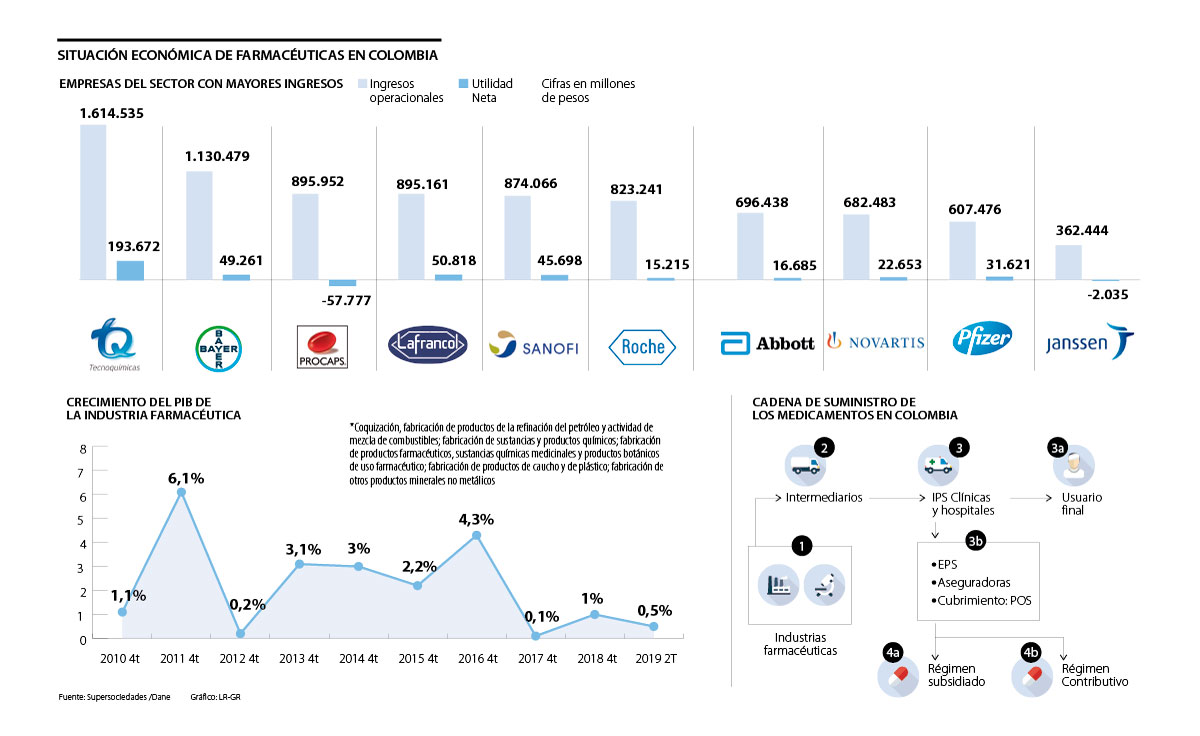
En primer lugar, una de las preocupaciones, en las que todas las industrias coinciden es que los trámites que requieren para trabajar, según lo establecido, no están siendo ágiles ni eficientes, pues algunos de ellos afirman que tienen renovaciones con más de dos años sin respuesta, además de requerimientos adicionales que antes no se tenían, lo que aumenta tiempos de evaluación, y en otros casos, se han tomado decisiones de no lanzar nuevas moléculas por falta de garantías en los tiempos y en los tipos de evaluaciones regulatorias que la entidad tiene.
Una consecuencia de ello, según lo expresado por una multinacional es que empiecen a caer algunos índices, como por ejemplo, el de inversión extranjera en Colombia, pues ellos representan gran parte de lo que impulsa el crecimiento de este indicador.
Esto claramente constituye un problema, no solo para el sector, sino para la economía en general, pues parte de la proyección económica de crecer por encima de 3%, se apalanca a través de la inversión extranjera y de la producción nacional, en la que también participan algunas de las industrias nacionales que manifestaron sus inconformidades.
Además de eso, algunas empresas informaron que no hay una coherencia entre las normas que dicta el Ministerio de Salud a través del Instituto Nacional de Salud y lo que hace el Invima, pues aunque ellos van en línea con estas entidades, lanzando al mercado productos con todo el marco legal vigente, le son negados los registros o renovaciones, provocando que estas incurran en gastos innecesarios, y, en el peor de los casos, pérdidas económicas.
LR también indagó acerca de la posibilidad de que por algún inconveniente entre las industrias y la entidad reguladora, se diera un desabastecimiento de medicamentos o, peor aún, que se generara un problema de salud pública. Una de las empresas consultadas respondió que a pesar de que están produciendo un medicamento indispensable para el tratamiento de una enfermedad compleja con una oferta muy reducida, en este momento tienen represada una maquinaria que no ha obtenido la certificación por parte del Invima necesaria para operar. Esto, sin duda, pone a la entidad en el centro de la mira, pues un retraso en trámites de este tipo puede repercutir en la salud de las personas que dependen de estas medicinas.
Por otro lado, un problema que destacan algunas farmacéuticas es que a pesar de que han buscado la manera de concretar una mesa de trabajo para buscar la solución entre las empresas del sector, gremios y el mismo Invima, la entidad pública no ha respondido a las solicitudes, ni tampoco se ha prestado a tratar de solucionar los problemas, que según las declaraciones de las empresas, son evidentes hasta para el mismo Invima, pues en algunos acercamientos ha aceptado las actuales coyunturas negativas por las que atraviesa.
El gremio que reúne a las empresas del sector, Afidro, reconoce que el Invima está atravesando por un proceso de transformación digital y además está en procesos de completar su planta de personal, lo que hace que se den las dificultades con los tiempos, pero recalcan su apoyo a la entidad para el fortalecimiento de las mejores prácticas reguladoras posibles, para así ofrecer a los pacientes un acceso más eficiente a las mejores opciones de medicamentos.
De parte de la cámara farmacéutica de la Andi, en cabeza de Ana María Vesga, esta situación está generando retrasos en lanzamientos de nuevos productos, además de posibles desabastecimientos, lo que en conjunto representa una barrera de acceso para los pacientes. No obstante, Vesga asegura que se viene trabajando para mejorar los tiempos y avanzar en la agilización de trámites.
Finalmente, es importante mencionar que LR realizó el acercamiento con el Invima, con el fin de conocer su versión, sin embargo, la entidad no se pronunció al respecto.
Recomendación de la OMS para entidades de vigilancia en la región
Los registros para medicamentos se dan y se renuevan a las industrias farmacéuticas, dependiendo la autoridad reguladora de cada país. En el estudio ‘Requisitos para el registro de medicamentos en las Américas’ que realizó la OMS en compañía de diferentes agremiaciones de la región como Afidro, y diferentes entidades de vigilancia de países de América Latina, incluido el Invima se recomendó el establecimiento de un periodo de validez del registro por cinco años, y que sea renovable por iguales periodos sucesivos.
La organización espera invertir hasta $400.000 millones en los próximos años y al menos $40.000 millones durante 2026
De acuerdo con la Aeronáutica Civil, Avianca cuenta con casi la mitad de estos permisos de aterrizaje y despegue en uno de los aeropuertos más importantes de la región
La utilidad neta de la compañía sumó cerca de $160.000 millones y aumento más de 64% frente al mismo periodo de 2025