MI SELECCIÓN DE NOTICIAS
Noticias personalizadas, de acuerdo a sus temas de interés
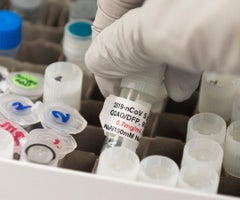
Se espera que los datos de eficacia y seguridad requeridos nos indiquen que tenemos un producto que responda a las necesidades
Los fabricantes de medicamentos que busquen una autorización de emergencia para una vacuna covid-19 tendrán que cumplir con un estándar de eficacia más alto de lo que normalmente se requeriría para tal autorización, dijo el jefe de la oficina de la Administración de Alimentos y Medicamentos de EE.UU. Que maneja las vacunas.
Por lo general, una autorización de uso de emergencia, o EUA, requeriría que una empresa demuestre que su producto puede ser efectivo. Peter Marks, director de la oficina de biológicos de la FDA, dijo que la agencia requerirá datos más sólidos sobre qué tan bien funciona una vacuna contra el coronavirus antes de otorgar una exención de emergencia, algo que llamó "EUA plus".
Marks dijo que el requisito de datos imitará más de cerca los estándares que se aplican a una solicitud para una aprobación regular. La vía de emergencia se utilizará principalmente para ayudar a eliminar algunos trámites y requisitos técnicos para llevar la vacuna a los estadounidenses más rápidamente, dijo.
Se espera que los datos de eficacia y seguridad requeridos “nos indiquen que tenemos un producto que va a hacer lo que está destinado a hacer”, dijo Marks en una investigación. Conferencia de América. Dijo que una vez que una vacuna llegue al mercado habrá un seguimiento de seguridad adicional.
La comunidad médica ha expresado su preocupación por permitir una vacuna en el mercado con autorización de emergencia, en lugar del proceso regular de aprobación de la FDA, particularmente dado el impulso del presidente Donald Trump para tener una inyección disponible para las elecciones del 3 de noviembre. Los funcionarios de carrera de la FDA, incluido Marks, escribieron un artículo de opinión el jueves en USA Today intentando tranquilizar a los escépticos de que están siguiendo la ciencia, no la política.
Hablando el jueves temprano en un evento del Economic Club of Washington, el comisionado de la FDA, Stephen Hahn, dijo cuando se le preguntó cuándo se podría autorizar una inyección que la agencia aún no ha recibido datos sobre ninguna de las vacunas en ensayos clínicos.
"No tengo una bola de cristal", dijo Hahn. “Sería realmente inapropiado para mí especular. No hemos visto los datos clínicos. No hay forma de que yo sepa posiblemente cuándo nos llegará eso".
Según LatAm Pulse, una encuesta realizada por AtlasIntel para Bloomberg News, el índice de aprobación de Milei subió a cerca de 40%
Gas provendría del proyecto Ksi Lisims LNG, una planta de exportación con un costo de US$7.200 millones en Columbia Británica
Un repunte de casi 20% en S&P 500 desde los mínimos provocados por la guerra dejó al índice en camino de su novena semana consecutiva de avance